妊婦のオメガ3脂肪酸摂取が将来の子の正常な脳機能の発現に影響を与えるならば…?
「私たちは食べたものでできている。私たちは食べたもの、そのものである。」
昨今、民放ではグルメ番組の放送が増えています。また、地方局でも飲食店の宣伝ばかり…
私たちは最後まで〝フルイ″にかけられている。そう感じるのは私だけでしょうか?
以下は2026年と、最新の論文です。
多くの日本人が毎日使っているサラダ油(菜種油や大豆油、コーン油なども含め)やマヨネーズ、マーガリン、加工食品中の植物油脂、市販のパンなどが脳に与える影響について警笛を鳴らしていますので一読されることをお勧めします。
なお、論文中に関連事項を追記しておりますのでご確認ください。
・必須脂肪酸の脳発生における役割に関する研究酒寄 信幸 2026年 79 巻 1 号 29-34 より引用
要旨:n-6 および n-3 多価不飽和脂肪酸(PUFA)は必須脂肪酸である。生体における n-6/n-3PUFA 組成比は様々な生理機能の調節に関与するが,現代の多くの国々において n-6 PUFA 摂取量は増加,n-3 PUFA 摂取量は減少している。
我々はこれまで,妊娠マウスにリノール酸高含有/α-リノレン酸低含有(高 LA/低ALA)飼料を投与すると,仔において大脳皮質グルタミン酸作動性ニューロンが減少することや,中脳ドパミン作動性ニューロンおよび扁桃体グルタミン酸作動性ニューロンが増加することを明らかにした。
さらに,高 LA/低 ALA を摂取した妊娠マウスの仔は,出産時から n-3 PUFA に富む飼料を投与して成長させても,成体において不安様行動の増加,社会性行動の減少,スクロース水の摂取量の増加といった行動異常を示すことを見いだした。
以上から,妊娠中の n-6 および n-3 PUFA の摂取バランスは胎仔脳の発生に作用し,将来の仔の行動にまで影響を及ぼすことが示された。
は じ め に
「医食同源」という言葉が示すように,健康の維持には栄養バランスの取れた食事が不可欠である。
しかし,脂質の摂取量は日本のみならず世界各国で増加しており,この 100 年間で食事に含まれる脂質の種類も劇的に変化している。そのため,脂質がヒトの健康に及ぼす影響を明らかにすることは,現代における重要な科学的課題である。
n-6 および n-3 多価不飽和脂肪酸(PUFA)は生体内で新規合成できないため,食物から摂取する必要のある必須脂肪酸である。これらの PUFA は生体内において生体膜の構成要素やシグナル伝達物質の前駆体などとして重要な役割を担う。
特に脳は脂質に富む器官であり,その乾燥重量の約 6 割を脂質が占めている。
一方,脳は脂質の質(種類)に関しても他の組織とは異なる特徴を示す。
脳における n-6 PUFA の多くはアラキドン酸(ARA)であり,n-3 PUFA のほとんどはドコサヘキサエン酸(DHA)である。他の組織では豊富に存在する α-リノレン酸(ALA)やエイコサペンタエン酸は脳にほとんど存在しない。
このような脳に特有の脂肪酸組成,特にDHA が脳に豊富に存在することは 1960 年代には見いだされており,1980 年代にはその機能的意義に関する研究が報告され,現在では情動や学習をはじめとする多様な脳機能の調節に脳内 DHA が重要な役割を担っていることが明らかになっている。
n-6 および n-3 PUFA は脳の発生・発達においても重要な役割を担っている。
早産児に DHA を投与することで神経発達スコアが改善することを示した介入研究や,妊婦における魚介類摂取量が児の神経発達の低下リスクを減少させることに関連することを明らかにした出生コホート研究などにより,妊婦における n-3 PUFA摂取が将来の子における正常な脳機能の発現に重要であることが示されてきた。
母親における n-3 PUFA 摂取が子の脳の発生・発達に作用する機序としては,「生後」脳の「発達」(主にシナプス形成)を DHA が促進することがよく注目されている。
(追記)
シナプス形成は、神経細胞の軸索が標的に到達し、相手細胞(樹状突起など)と連結して神経回路を作るプロセスです。
以下のように「ニューロン層の厚さが減少する」時、神経回路の結びつきが弱いことを意味します。
これは簡単に言うと、正常ならばパソコンの演算処理ができる一方で、ニューロン層の厚さが減少すると電卓に、さらに薄くなると手の指を使った足し算や引き算しかできなくなるなど、脳の処理能力低下に繋がります。
一方で,n-3 PUFA が「胎児」脳の「発生」にどのような影響を及ぼすのかについては解明が遅れていた。
Kawakita et al. は,ラット胎仔大脳皮質原基に由来する培養神経幹細胞に DHA を添加するとニューロン分化が亢進することを報告し,DHAが脳発生を制御する因子であることが示された。
さらにCoti Bertrand et al. は,n-3 PUFA 欠乏飼料を投与した妊娠ラットの胎仔において大脳皮質のニューロン層の厚さが減少する(つまりニューロン数が減少する)ことを明らかにし,正常な脳発生に n-3 PUFA が必要であることが組織レベルでも明らかにされた。
(追記)
・健やかな脳の発生・発達と脂質 酒寄 信幸, 大隅 典子 2016年 21 巻 4 号 4_59-4_62 より引用
n-6 PUFA過多/n-3PUFA欠乏飼料を摂取した仔マウスの神経幹細胞はニューロン産生が減少しており、その分アストロサイトという神経細胞の補助を担うグリア系の細胞が多く産生された。
これにより、n-6 PUFA過多/n-3 PUFA欠乏飼料が神経幹細胞のニューロン・グリア産生バランスを崩し、分化能をグリア細胞へ偏らせることによって大脳新皮質のニューロン数の減少につながったことが示された。
我々は Kawakita et al. および Coti Bertrand et al. の報告を受け,n-3 PUFA が脳発生を制御する発生学的メカニズムの解明を目指し,研究に着手した。
本稿では,妊娠中に摂取する n-6 および n-3 PUFA の両方が胎児脳の発生に作用し,子の将来の行動にまで影響を及ぼすことを明らかにしてきた我々の報告を紹介する。
1.胎児脳の発生における n-6 およびn-3 PUFA の役割
n-6 および n-3 PUFA は生体内において輸送タンパク質や代謝酵素を共有しているため,PUFA 間で競合が起こる。そのため,個々の摂取量だけでなく生体におけるバランス(n-6/n-3 PUFA 組成比)も様々な生理機能の調節に関与する。
ヒトは n-6 PUFA と n-3 PUFA を概ね同量摂取しながら進化してきたと考えられているが,1900 年代から n-6 PUFA 摂取量の増加と n-3 PUFA摂取量の減少が進行している。
我々は,ラット胎仔大脳皮質原基に由来する培養神経幹細胞に ARA(アラキドン酸) を添加するとアストロサイト分化が亢進し,DHA を添加するとニューロン分化が亢進することを報告し,大脳皮質の神経幹細胞に対して ARA と DHA が異なる機能を有することを明らかにした。
そこで,我々は n-6 およびn-3 PUFA の両方に着目し,妊娠中に摂取する PUFA のバランスが胎仔の脳発生に及ぼす影響とその作用機序を明らかにする研究を行った。
まず我々は,リノール酸(LA:オメガ6)および ALA(α-リノレン酸:オメガ3) が総脂肪酸に対してそれぞれ 20.7%および 9.4%含まれるコントロール飼料(カノーラ油を配合),または LA およびALA がそれぞれ74.3%および0.3%含まれる高 LA/低ALA 飼料(ハイリノール紅花油を配合)を妊娠マウスに投与し,胎仔の脳の発生学的解析を行った。
コントロール飼料を投与した妊娠マウスの胎仔と比べ,高 LA/低 ALA 飼料を投与した妊娠マウスの胎仔において,脳における ARA の増加と DHA の減少が起こることを確かめた。
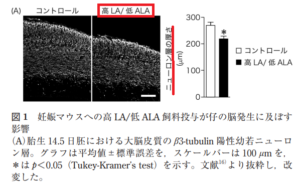
さらに,高 LA/低 ALA 飼料を投与した妊娠マウスの胎仔の大脳皮質において,Coti Bertrand et al. の報告と同様にニューロン層の厚さが減少することを見いだした(図 1A)。
また,高 LA/低 ALA 飼料を投与した妊娠マウスの仔の生後脳においても組織学的解析を行い,大脳皮質一次運動野,一次体性感覚野,一次視覚野においてグルタミン酸作動性ニューロンの数が減少することを明らかにした。
次に,我々はグルタミン酸作動性ニューロン産生が阻害された機序を明らかにするため,神経幹細胞の分化能の解析や液体クロマトグラフダンデム質量分析計(LC-MS-MS)を用いた胎仔脳の脂質メタボロミクス解析を行った。
誌面の都合上,詳細は割愛するが,高 LA/低 ALA 飼料を投与した妊娠マウスの胎仔の脳において,ARA に由来する代謝物と DHA に由来する代謝物の量のバランスが崩れ,神経幹細胞のニューロン分化の低下とアストロサイト分化の亢進が起こり,大脳皮質における各ニューロン層の正常形成が妨げられることを見いだした。
(追記)
1973~2012年度の40年間で,知的障害児の出生千当たり発生率は重度では増加していなかったが中軽度障害で増加がみられ,1993年頃を境に最近の20年間の増加が著しかった。
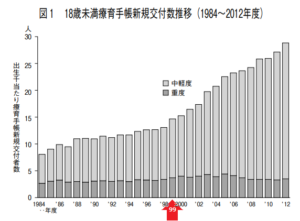
重度知的障害児の発生率は出生千当たり 2 ~3 人で過去30年間ほとんど変化していないが,中軽度知的障害児の発生割合は1999年度頃より急増している。
1984年度当時,知的障害児の発生率は0.8%くらいだったが2012年度には 3 %に近づいており,なおも増加傾向にある。
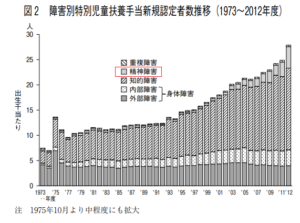
身体障害は内部障害にやや増加傾向がみられるものの,外部障害の発生率は40年間一定しており,近年ではむしろ減少傾向さえみられる。対して知的障害は1993年度頃より急増しており,さらに興味深いことは精神障害の発生率も2002~2003年度頃から増加傾向にある。
(図 2 )のうち知的障害について程度別に示したものが(図 3 )である。
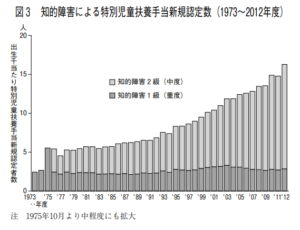
ここでも重度の発生率は40年間ほとんど一定であるが,中程度の知的障害の発生率が1993年度頃より急増している。
(追記)
上記論文では、この知的障害の発生について次のように結論付けています。
「各年の中程度知的障害の発生率は,数理モデルを適用することにより母の平均年齢と出生時体重の 2 要因だけで,ほぼ完全に説明される。
近年では出生時体重の減少は止まっているが,母年齢の高齢化はなおも進行しており,知的障害児の割合は今後も増加すると予想される。」
では、本当の原因はどこにあるのでしょうか?
それは、以下の論文で明らかです。
(追記)
妊娠初期の着床期の子宮内膜や分娩期の子宮頸管、子宮筋、卵膜には炎症性メディエーターの活性化が生じることが知られている。
特に、分娩期には子宮-卵膜内のマクロファージや好中球の集積とともに炎症性サイトカイン、プロテアーゼの働きが亢進して、子宮頸管の熟化(組織間質の膠原繊維の変化による軟化)、子宮筋の収縮、卵膜の破綻(破水)が生じることで分娩開始起点となる。
炎症性プロスタグランジン(PG)の中で PGE2 やPGF 2αは分娩進行に関わる中心的な脂質メディエーターであり、人工的に分娩を誘導する処置である分娩誘発では、頸管熟化および子宮収縮の促進を目的として、炎症性 PGの投与が行われる。
これらの炎症性 PG はオメガ 6PUFAs であるアラキドン酸を起点とした代謝経路により産生され、アラキドン酸カスケードと称される。
・子宮の炎症制御における脂質メディエーターの役割 ―オメガ3脂肪酸を中心に 永松 健 2022年 31 巻 1 号 30-35
(追記)
オメガ6過剰かつオメガ3不足の食生活は、体内に過剰な炎症性プロスタグランジン(PG)を産生します。そのため…
・妊娠初期:炎症性PGが受精卵の着床を妨げます。これが不妊の主因です
・妊娠中:炎症性PGが子宮収縮を促進し早産(流産も)となります
・早産児は、脳が正常に発達する以前に生まれています。これが知的障害が増えている主因です。
・授乳期:母乳中のDHAが不足しているため、母は産後うつに、児は脳の正常な発達を妨げることになります
我が子や孫など、子孫の将来を心配される方は「本当の妊活!」をお役立てください。
n-6 および n-3 PUFA のバランスが大脳皮質の発生を調節するメカニズムの一端を明らかにした。
上述した研究は大脳皮質を対象としたものだが,n-3PUFA 欠乏飼料をラットに投与すると脳内報酬系の中枢である中脳腹側被蓋野におけるドパミン作動性ニューロンからのドパミン放出が増加することが知られているため,我々は妊娠中に摂取する n-6 および n-3 PUFA のバランスが脳内報酬系の発生にも影響するのではないかと考え,妊娠マウスに高 LA/低 ALA 飼料を投与し,胎仔中脳における発生学的解析を行った。
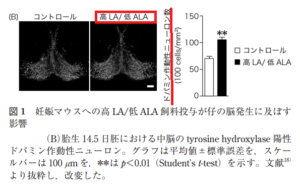
興味深いことに,コントロール飼料(当論文では AIN-93G 飼料)を投与した妊娠マウスの胎仔と比べ,高 LA/低 ALA 飼料を投与した妊娠マウスの胎仔においてドパミン作動性ニューロンの数が増加していた(図 1B)。
(追記)
ドパミンは脳内で「やる気・快楽・報酬・運動機能」に関与する神経伝達物質で、3大幸せホルモンの一つです。目標達成や快感時に放出され、モチベーションを高めます。不足するとパーキンソン病やADHD様の症状が出やすく、過剰だと統合失調症や依存症のリスクに関与します。
報酬系:「こうすれば儲かる(かもしれない…)」というときに最も活性化する。(予期報酬と呼びます)ギャンブル依存症やゲーム依存症がそのひとつで、前者は「この馬券を買えば儲かる(かもしれない…)」というとき、後者は「これでこのステージをクリアできる(かもしれない…)」というときにドバドバとドパミンが大量分泌されます。
ギャンブル依存やゲーム依存のヒトは仕事や勉強など前向きな行為に対する集中力が低下する一方で、競馬新聞による馬券検討やゲームプレイ時にはとても集中力が高まります。これがドパミンの大量分泌による効果です。
したがって、これら依存症の対策は簡単です。
オメガ6の摂取量を大幅に減らし、オメガ3を十分に摂取する。10日間チャレンジをお勧めします。
また,成体脳における PUFA 組成の高 ARA/低 DHA 化によって不安様行動が増加することが報告されていることに着目し,負の情動発現の脳内制御中枢である扁桃体基底外側核におけるグルタミン酸作動性ニューロンの発生に対する高 LA/低 ALA 飼料投与の影響も解析した。
コントロール飼料を投与した妊娠マウスの仔と比べ,高LA/低 ALA 飼料を投与した妊娠マウスの仔は扁桃体基底外側核におけるグルタミン酸作動性ニューロンの数が増加していた。
(追記)
扁桃体は脳内の「感情の司令塔」として機能します。特に恐怖、不安、不快感などの情動反応の処理、ストレスに対する危機管理、感情を伴う記憶の形成(恐怖記憶)に重要な役割を果たします。
危険を察知し、「闘争・逃走・すくみ」の反応を瞬時に引き起こすため、生存に不可欠な「原始的な脳(爬虫類脳的機能)」として機能し、時に理性を失わせる「扁桃体ハイジャック」を引き起こします。
扁桃体ハイジャックの例:高所恐怖症や閉所恐怖症、大きな音で身がすくむ(風でドアが閉まった音など)
大脳皮質グルタミン酸作動性ニューロン産生と中脳ドパミン作動性ニューロン産生・扁桃体基底外側核グルタミン酸作動性ニューロン産生とで真逆の結果が得られた原因は不明であり,それぞれの脳領域でARA および DHA が異なる発生プロセスを制御する可能性が示唆された。
2.妊娠中に摂取する n-6 および n-3 PUFA が子の将来の行動に及ぼす影響
高 LA/低 ALA 飼料や n-3 PUFA 欠乏飼料をマウスやラットに胎仔から成体まで長期投与すると,成体脳における ARA の増加と DHA の減少が起こり,シナプス伝達やその可塑性に異常が生じ,結果として情動機能や学習機能の正常な調節が阻害されることが広く知られている。
(追記)
発達障害脳の特性により発達の仕方に偏りがあり、幼児期から日常生活やコミュニケーションに困難が生じる、生まれつきの脳機能障害とされています。
主なタイプにASD(自閉スペクトラム症)、ADHD(注意欠如・多動症)、LD(学習障害)がありますが、情動機能が阻害されれば自閉スペクトラムやADHD,学習機能が阻害されれば学習障害となると想像するのは私だけでしょうか?
また、幼少期は問題が無かったのに、年を重ねて問題が生じ大人になって発達障害と診断されるヒトが増えています。これもまた、上記の「高 LA/低 ALA 飼料や n-3 PUFA 欠乏飼料をマウスやラットに胎仔から成体まで長期投与すると、結果として情動機能や学習機能の正常な調節が阻害される」で説明できます。
したがって、私は発達障害もまた、オメガ6過剰摂取およびオメガ3の大幅な摂取不足が原因のひとつだと確信しています。10日間チャレンジをお勧めします。
では,n-6 および n-3 PUFA の摂取バランスへの介入を妊娠期に限定した場合,子の将来の行動に変化は生じるのだろうか。
まず我々は,高 LA/低 ALA 飼料の長期投与によって起こる行動異常の中でもよく知られた不安様行動の増加について検証した。
ここでは妊娠マウスにコントロール飼料または高 LA/低 ALA 飼料を投与し,出産後10 日目から両群の母マウスに AIN-93G 飼料を投与した(生後 10 日目の仔マウスの脳の発生段階は,ヒトの出産直後の新生児の脳の発生段階に相当するため)。
その後,両群の仔を 3 週齢で離乳し,以降は仔に AIN-93M 飼料を投与し,仔が成体になった後に不安様行動を解析した。
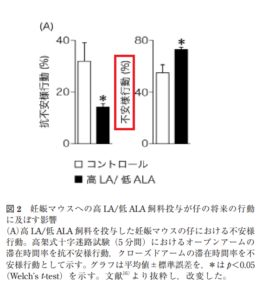
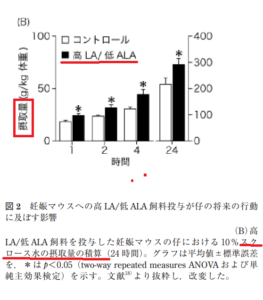
すると,コントロール飼料を投与した妊娠マウスの仔と比べ,生後 10 日目まで高 LA/低 ALA 飼料を投与した妊娠マウスの仔における不安様行動が増加した(図 2A)。
なお,妊娠マウスにコントロール飼料または高 LA/低ALA 飼料を投与し,出産時から両群を CE-2 飼料で飼育した場合でも,高 LA/低 ALA 飼料を投与した妊娠マウスの仔における不安様行動は増加した。
以上から,妊娠期の母親における n-6 および n-3 PUFA の摂取バランスは仔の将来の情動機能の一部に決定的な影響を及ぼすことが示された。
1.で述べた通り,高 LA/低 ALA 飼料を投与した妊娠マウスの仔において扁桃体基底外側核におけるグルタミン酸作動性ニューロンの数が増加するため,負の情動発現の脳内制御中枢における発生異常によって不安様行動の増加が引き起こされた可能性が考えられる。
次に我々は,食中 PUFA 組成の高 n-6/低 n-3 化の進行は肥満人口の増加と正の相関を示すことから,妊娠中の n-6 および n-3 PUFA 摂取バランスが仔の摂餌行動に影響を及ぼすかを検証した。
ここでは妊娠マウスにコントロール飼料(当論文では AIN-93G 飼料)または高LA/低 ALA 飼料を投与し,出産時から両群にコントロール飼料を投与し,仔を成体まで飼育した。両群の仔の体重やコントロール飼料の摂餌量に群間差はなかったが,コントロール飼料を投与した妊娠マウスの仔と比べ,高LA/低 ALA 飼料を投与した妊娠マウスの仔はスクロース水の摂取量が増加した(図 2B)。
上述の通り,高 LA/低 ALA 飼料を投与した妊娠マウスの胎仔において中脳ドパミン作動性ニューロンが過剰に産生されるため,脳内報酬系における発生異常がスクロース水の摂取量を増加させる原因となった可能性がある。
さらに我々は,妊娠期における n-6 および n-3 PUFAの摂取バランスが子の将来の行動に及ぼす影響の全容を解明するため,妊娠マウスにコントロール飼料または高LA/低 ALA 飼料を投与し,出産時から両群に CE-2 飼料を投与し,仔が成体になった後に網羅的な行動解析を実施した。
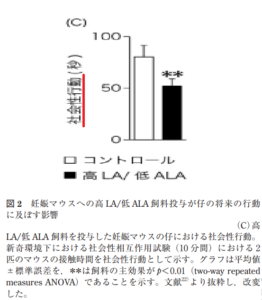
これにより,コントロール飼料を投与した妊娠マウスの仔と比べ,高 LA/低 ALA 飼料を投与した妊
娠マウスの仔では社会性行動が減少し(図 2C),一方で認識記憶は向上することを見いだした。
なお,高 LA/低ALA 飼料を投与した妊娠マウスの雌の仔では自発運動量の増加や空間記憶学習における行動柔軟性の低下までみられ,発生する行動異常に性差があることも分かった。
以上から,妊娠期における n-6 および n-3 PUFA の摂取バランスに関連する仔の行動様式の全容を明らかにした。
お わ り に
妊娠マウスにコントロール飼料または高 LA/低 ALA飼料を投与し,出産時または出産後 10 日目から n-3PUFA を含有する飼料(AIN-93G 飼料や CE-2 飼料)を両群の母マウスに投与し,離乳後も n-3 PUFA 含有飼料(AIN-93M 飼料や CE-2 飼料)を両群の仔に投与した場合,仔の成体脳における脂肪酸組成にほとんど群間差がみられない20)22)。
そのため,成体脳における脂肪酸組成に依存しない行動異常が観察されたと考えられる。
今後,各種行動異常の背景にある脳の器質的変化を精緻に特定するとともに,それらがどのような神経活動の異常を引き起こすのかを解明していきたい。
最近,環境省の「子どもの健康と環境に関する全国調査」により,日本人の妊婦における n-6/n-3 PUFA 摂取比の増加は児における一部の神経発達スコアの低下リスクの増加と関連することが明らかにされた。
同様の結果は韓国人を対象にした調査においても報告されている。
興味深いことに,妊婦における n-6 PUFA や n-3PUFA の摂取量自体は児における神経発達スコアの低下リスクを減少させることが報告されており,動物実験においても n-6 PUFA の摂取と脳内 ARA が生後脳の正常な発達に重要であることを示す知見が示されている。
これまで脳の発生・発達を調節する PUFA の研究は n-3 PUFA の摂取量と脳内 DHA に着目するものが多かったが,これらの研究によって n-6 PUFA の摂取量や n-6 および n-3 PUFA の摂取バランスにも着目する重要性が改めて示された。
n-6 および n-3 PUFA がどのように脳の発生・発達を制御し,正常な脳機能の発現に寄与するのかを明らかにすることは,現代社会において増加する脳関連疾患の病態解明にもつながる可能性のある重要な課題である。
このままの食生活が続けば、おそらく後30年で日本は滅びることになるでしょう。
もう、待ったなし!
一日も早く、こういった事実が周知されることを心から願っています。